近日,智因东方兄弟公司——北京卡替医疗技术有限公司同株洲市中心医院血液科合作,运用个体定制化多靶点免疫细胞治疗技术,治疗一位血管免疫母T细胞淋巴瘤(AITL)患者,获得成功。
AITL是外周T细胞淋巴瘤(PTCL)的一种亚型。这位患者是一位72岁的老大爷,患病后被担架抬到医院,经传统治疗无效,全身淋巴结肿大,且出现了噬血细胞综合征的现象。这种疾病预后发展非常凶险,患者身体每况愈下,但传统治疗方法已束手无策。那么,免疫细胞治疗能否在此时派上用场呢?
株洲市中心医院血液科胡国瑜主任在同北京卡替医疗团队讨论研究后,决定尝试采用一种尖端、前沿的技术——个体定制化多靶点肿瘤免疫细胞治疗。
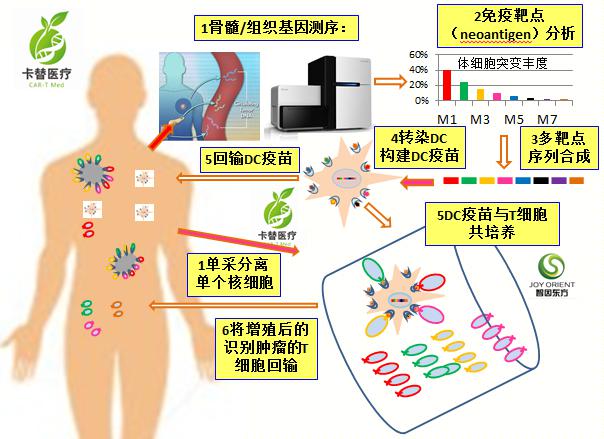
这种疗法的大体过程是,先通过基因测序,得到患者肿瘤的体细胞突变谱,再根据患者个性化的肿瘤突变谱,选择一些可以作为治疗靶标的突变(也叫作新抗原,neoantigen),在体外“训练”并筛选能识别这些新抗原的T细胞(这些T细胞就是优中选优的抗癌“特种兵”),把这些T细胞在体外进一步扩增后,回输给患者。
考虑到患者的疾病特点和自身状况并不适合采用自体细胞(源自患者自身的细胞)的过继性免疫治疗,故胡主任经同北京卡替团队讨论研究后决定,采用源自患者女儿的半相合异体的细胞,来制备多靶点T细胞,实施个体定制化免疫治疗。
2017年8月16日,患者接受了由北京卡替医疗制备的半相合异体多靶点T细胞的输注治疗。输注后,患者身体没有任何不适的感觉,也没有出现CAR-T疗法常见的高热现象,医生曾一度担心是不是没有疗效。但是奇迹很快出现了。
短短一周内,患者的精神状况和身体素质明显改观,从食欲不振到食欲大开,从卧床不起到能下地散步,CT显示患者全身的淋巴结肿大已全部消失,肿瘤相关的生化检查全部正常,治疗前的异常的炎性因子和粒细胞指标,在治疗后也全部恢复正常。2017年8月22日,患者顺利出院。直至目前的回访,患者精神矍铄,神采奕奕,已完全不似原先的患病状态。
对于AITL,传统治疗手段效果大多不尽理想。本例运用半相合异体的个体定制化多靶点免疫治疗技术所获得的成功,对于AITL的治疗史来说,应属全球首例。
回顾本例,对于这种T细胞肿瘤,免疫细胞治疗面临两大难点。
第一个难点是这种肿瘤目前没有通用治疗靶点,故无法应用CAR-T技术。CAR-T技术堪称当前血液肿瘤疗法的明星,但它在这种疾病面前却是英雄无用武之地。因为目前的CAR-T技术,都是只能识别肿瘤细胞表面的单一靶点,故适用范围有限,一般只能对治某一类的血液肿瘤,比如靶向CD19、CD20的CAR-T对治的大多是B细胞系的肿瘤(如B细胞白血病、淋巴瘤等),靶向BCMA的CAR-T对治的是多发性骨髓瘤这类浆细胞肿瘤。但目前尚未有对治T细胞肿瘤的CAR-T技术。
第二个难点是,T细胞作为过继性免疫细胞治疗的主力军,用来治疗肿瘤的T细胞(即我方)本身就有一部分是肿瘤细胞(即敌方),这是免疫治疗对治T细胞肿瘤的普遍存在的难点。另外,这类患者在做免疫治疗前,大多已经历过反复化疗,其免疫细胞状态也已大不如前。因此用患者自身的T细胞来制备免疫细胞,存在天然的缺陷性。
那么在这个案例中,个体定制化多靶点免疫治疗技术为何能大获成功呢?因为相对于固定单个靶点的CAR-T技术,个体定制化多靶点免疫治疗技术有几大优势和特点:
一是这种疗法在适用范围上几乎可以是不限癌种的广谱手段。这种技术不依赖于肿瘤的固定靶标,而是借助基因测序获得个体化靶标,故在适用范围上突破了固定靶标疗法的天然局限性。2017年7月《Nature》同一天刊发两篇关于黑色素瘤的个体化癌症免疫治疗的震撼性成功报道,结合本例的成功,在一定程度上说明无论是实体瘤还是血液肿瘤,只要肿瘤突变数目足够多,理论上就都可以适用于这种疗法, T细胞肿瘤自然也不例外。
二是这种多靶点治疗技术突破了单靶点的局限,理论上疗效会更有保障。肿瘤突变是一个复杂的动态的突变谱,一个患者的肿瘤突变数量可多达成千上万,而且其丰度还在不断变化,新突变在不断产生。就好比我们遇到一群狼,单靶点治疗技术局限性在于只打其中一只狼(只对治一个突变靶标),那么即便这一只狼被打死,其他狼也会围上来把人咬死(携带其他突变的肿瘤细胞会继续生长)。而多靶点技术则是同时打多只狼(同时对治多种突变的肿瘤细胞),故理论上疗效会更有效且更持久。
三是这种疗法在机制上比CAR-T更安全。CAR-T技术是对T细胞进行了基因工程性改造,给T细胞表面加上了嵌合抗体,同时连上了共刺激因子,尽管疗效显著,但其副作用——细胞因子风暴(CRS)则是难以避免的。而个体定制化多靶点疗法对T细胞没有做任何工程性改造,只是进行了巧妙的筛选,把能特异识别肿瘤的T细胞筛选出来并扩增,所以在机制上比CAR-T更安全。本例患者治疗后没有出现任何不良反应,即体现出了这种疗法的高度安全性。
四是这种疗法是高度个性化的。每个患者的治疗靶点都是各不相同的,最终的产品,无论是个体化癌症疫苗,还是个体化多靶点T细胞,都是个体化“手工打造”,所以被称为“个体定制化多靶点”治疗技术。
因此,个体定制化多靶点技术可以天然的解决上述第一个难点,而采用来自患者女儿的半相合异体的细胞,来制备多靶点T细胞,则是解决第二个难点的大胆而精明的对策。
本例的成功,不仅为T细胞肿瘤患者带来福音,更重要的是它再一次验证了个体定制化多靶点免疫治疗技术的广谱性和可行性,因此也将会是其他癌种患者的福音。

关于北京卡替医疗:
北京卡替医疗技术有限公司(CAR-T Med Co. Ltd.)成立于2015年,汇聚全球顶尖科学家加盟,拥有CAR-T(靶向CD19/20,BCMA,EGFRviii等)、TCR-T(靶向NY-ESO1等)、TIL、PD1/PDL1单抗、个体化多靶点neoantigen技术(包括癌症疫苗技术及新抗原反应性T细胞技术)等多种前沿免疫治疗技术于一身,创立个体定制化且集合单靶点、多靶点、精准、动态、广谱、高效等多种优势及特点,熔多种技术于一炉的肿瘤综合免疫治疗整体解决方案。


